Dos niños de La Fe de Valencia con distrofia de Duchenne se quedan sin tratamiento
Los niños son de la Comunidad de Castilla y León que no asume el gasto del fármaco
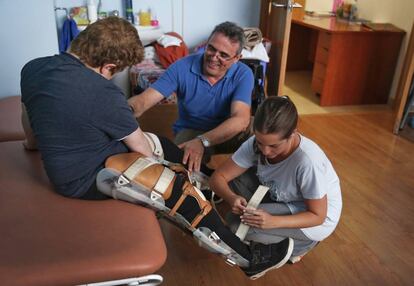
Dos de los nueve niños con distrofia muscular de Duchenne (DMD), que participan en un ensayo clínico con un fármaco experimental para tratar esta enfermedad genética en el Hospital La Fe de Valencia, se quedan sin medicación el mes que viene. La investigación ha finalizado y el ataluren, nombre del principio activo del tratamiento, ha sido aprobado por la Agencia Europea del Medicamento (AEM) para su uso provisional porque hay indicios de su eficacia en ralentizar la progresión de esta distrofia.
Los tres pequeños valencianos, los dos vascos y los dos portugueses continuarán con la medicación porque sus comunidades autónomas y el país vecino estudian financiar los nuevos lotes de tratamiento. Pero los dos niños de Castilla y León no lo tienen asegurado.
Los médicos, responsables del ensayo, y los familiares de los niños con Síndrome de Duchenne exigen al Ministerio de Sanidad que negocie con el laboratorio que produce el medicamento, PTC Therapeutics Internacional Limited, una situación transitoria hasta que concluyan todas las investigaciones que quedan por hacer para que todos tengan la medicación por igual.
El doctor Juan Vílchez, jefe del Servicio de Neurología de La Fe, denuncia que “no hay equidad ni igualdad territorial”. Los niños vinieron a Valencia buscando el ensayo clínico y si no se lo damos, la progresión de la enfermedad les llevará a una “situación irreversible”, señala el neurólogo. En España, los laboratorios seleccionaron dos centros para probar el fármaco, uno de ellos era La Fe.
Desde enero de 2017, la AEM autoriza el uso del fármaco y le concede una licencia provisional como único tratamiento para el Síndrome de Duchenne con la condición de hacer un seguimiento anual. Países como Italia, Francia y Gran Bretaña han asumido la financiación del tratamiento para sus pacientes y han negociado con el laboratorio el precio de venta. Sin embargo, en España el Ministerio de Sanidad se ha inhibido y deja el tema en manos de las administraciones autonómicas.
El Hospital La Fe tiene tratamiento para los niños hasta julio. Una vez se terminen las dosis del fármaco se tendrá que comprar al laboratorio. El doctor Vílchez pide que España haga lo mismo que los otros países y pacte con el laboratorio un precio asequible para uso compasivo -utilizar un medicamento en fase de investigación clínica de forma excepcional-, de forma que se pueda continuar tratando a todos los niños que han participado en la investigación.
Los ensayos clínicos con ataluren, asegura el doctor Vílchez, han ayudado a conocer mejor una enfermedad muy compleja. Esta enfermedad genética impide al cuerpo generar la proteína básica de la estructura muscular, lo que produce debilitamiento progresivo y atrofia. Los síntomas se detectan durante la infancia y empeoran rápidamente. Los niños van perdiendo fuerza en sus músculos, incluido el cardíaco, hasta que requieren de silla de ruedas entre los 10 y los 13 años. En la adolescencia suelen requerir asistencia respiratoria.
De la investigación se deduce que hay momentos, en la fase inicial de la enfermedad, “donde el medicamento es muy eficiente”. Es un tratamiento indicado antes de que los niños alcancen un grado de debilidad tal que se ven obligados a ir en silla de ruedas. “Pero se ha de seguir investigando”, concluye Vílchez.

Ataluren modifica la lectura del código genético alterado y ralentiza la progresión de la enfermedad al impedir que las células lean la mutación. El cuerpo sigue fabricando la proteína esencial para el buen funcionamiento muscular, la distrofina, aunque es un poco diferente. El alcance final del estudio es averiguar si esta nueva distrofina cumple con su cometido parcial o no y el otro aspecto del ensayo es ampliar la muestra a otros afectados en diferentes fases del síndrome.
Los niños afectados no disponen de tratamiento alternativo. El Hospital La Fe de Valencia es uno de los centros españoles de referencia para el tratamiento de esta enfermedad, que afecta principalmente a los varones, con una incidencia de uno por cada 3.500 nacidos. En la Unión Europea hay 25.000 personas con la enfermedad, según fuentes del Ministerio de Sanidad.